Dans un monde où les troubles anxieux et dépressifs touchent des centaines de millions de personnes, la recherche scientifique explore des pistes thérapeutiques innovantes. Parmi elles, l’étude de l’axe microbiome-intestin-cerveau révolutionne notre compréhension de la santé mentale. Loin d’être de simples organes de digestion, nos intestins abritent un écosystème complexe de 100 000 milliards de microorganismes qui dialoguent en permanence avec notre cerveau, influençant nos émotions, notre cognition et notre comportement.
Un dialogue bidirectionnel entre deux cerveaux
L’axe intestin-cerveau représente un système de communication bidirectionnelle extraordinairement complexe qui relie le système nerveux central au système nerveux entérique. Ce dernier, souvent surnommé notre « deuxième cerveau », contient entre 200 et 600 millions de neurones tapissant la paroi intestinale, soit davantage que la moelle épinière 1. Cette connexion ne se limite pas à la transmission d’informations sur la digestion : elle module profondément notre état émotionnel et nos processus cognitifs.
Selon le Dr Sean Spencer, gastro-entérologue et chercheur à l’Université de Stanford, « l’interaction complexe entre notre microbiome et notre cerveau témoigne de l’interconnexion remarquable du corps. Il ne s’agit pas seulement de santé intestinale ou de santé mentale, mais de la manière dont chacune influence l’autre de façon profonde » 1.
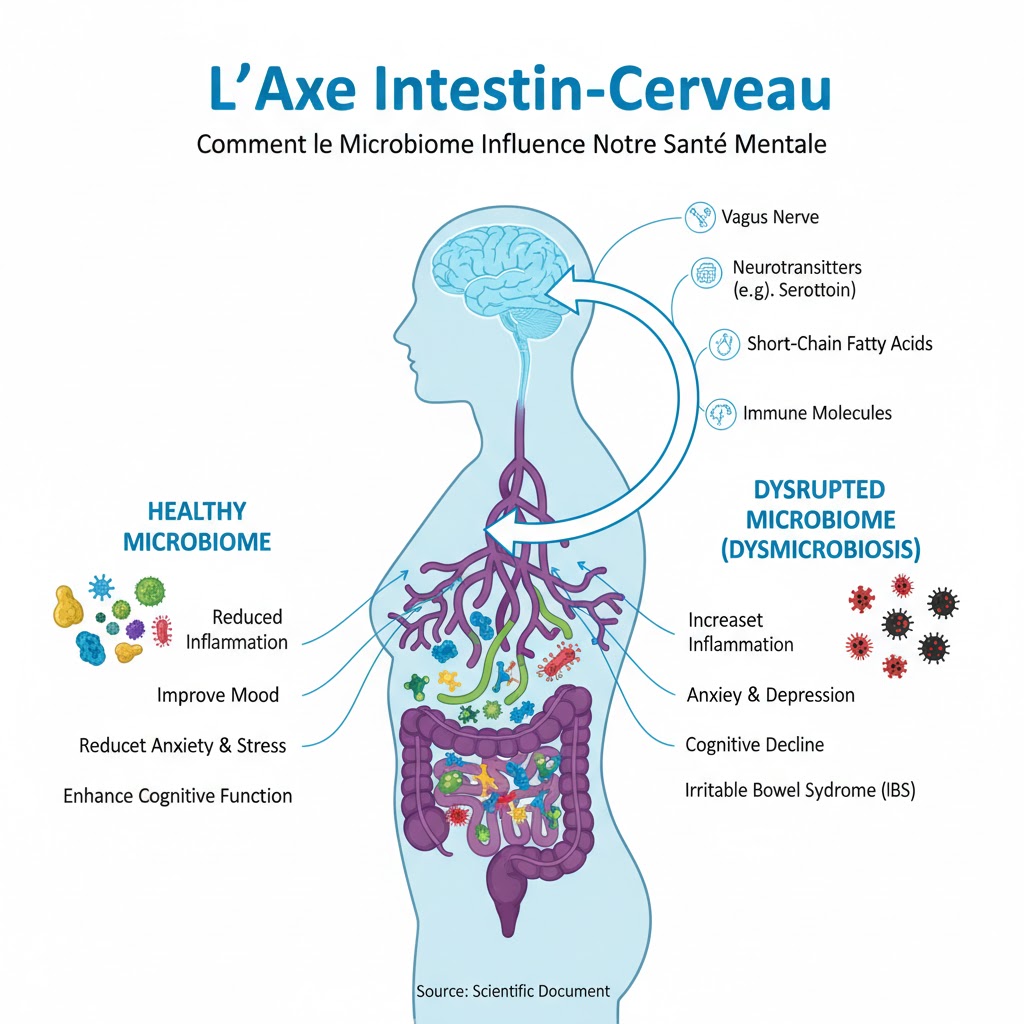
Cette communication s’effectue par quatre voies principales : neurologique (via le nerf vague), endocrinienne (hormones et peptides), humorale/métabolique (métabolites microbiens) et immunitaire (cytokines et cellules immunitaires) 2. Chacune de ces voies peut influencer les centres cérébraux responsables de la régulation émotionnelle, de la mémoire et de la cognition.
Le microbiome intestinal : un acteur clé de notre santé mentale
La découverte récente que le microbiome intestinal affecte la santé et la maladie a catalysé une explosion de recherches multidisciplinaires 3. Le microbiome, composé principalement de bactéries appartenant aux phyla Firmicutes et Bacteroidetes, produit une multitude de neurotransmetteurs, d’hormones et de métabolites bioactifs qui peuvent traverser la barrière hémato-encéphalique et moduler l’activité cérébrale.
Des études révolutionnaires utilisant des transplantations fécales de patients psychiatriques vers des rongeurs axéniques (dépourvus de microbiote) ont démontré l’induction de symptômes similaires à ceux des donneurs 4. Inversement, certains probiotiques ou transplantations fécales provenant de donneurs sains se sont révélés efficaces pour atténuer les symptômes chez des patients atteints de troubles psychiatriques 4. Ces résultats suggèrent fortement que le microbiome intestinal joue un rôle crucial dans l’apparition et la modulation des troubles psychiatriques.
Les acides gras à chaîne courte : messagers moléculaires essentiels
Parmi les métabolites produits par le microbiome, les acides gras à chaîne courte (AGCC) – acétate, propionate et butyrate – occupent une place centrale dans la communication intestin-cerveau. Ces molécules résultent de la fermentation des fibres alimentaires par les bactéries intestinales et constituent bien plus qu’une simple source d’énergie pour les cellules du côlon 5.
Environ 500 à 600 mmoles d’AGCC sont produites quotidiennement dans l’intestin, selon un ratio approximatif de 60:20:20 pour l’acétate, le propionate et le butyrate respectivement 5. Ces AGCC traversent la barrière hémato-encéphalique grâce aux transporteurs monocarboxylates exprimés en forte concentration par les cellules endothéliales 6. Leur présence dans le liquide céphalo-rachidien humain a été confirmée, avec des concentrations physiologiques de 0-171 µM pour l’acétate, 0-6 µM pour le propionate et 0-2,8 µM pour le butyrate 6.
Les AGCC exercent des effets neuroprotecteurs multiples. Le butyrate, en particulier, possède des propriétés anti-inflammatoires puissantes, éteignant les processus inflammatoires dans l’intestin comme dans le cerveau 7. Ces molécules régulent également l’expression des enzymes clés de la synthèse des neurotransmetteurs : la tryptophane 5-hydroxylase (impliquée dans la production de sérotonine) et la tyrosine hydroxylase (impliquée dans la synthèse de dopamine, noradrénaline et adrénaline) 8.
Des études récentes sur des modèles animaux de dépression induite par hypoperfusion cérébrale chronique ont démontré que l’administration d’un mélange d’AGCC atténue la neuroinflammation hippocampique et l’apoptose neuronale, tout en améliorant le déclin cognitif et les comportements dépressifs 6. Ces découvertes ouvrent des perspectives thérapeutiques prometteuses pour traiter les troubles de l’humeur par la modulation du microbiome.
Le nerf vague : autoroute de la communication intestin-cerveau
Le nerf vague représente le composant principal du système nerveux parasympathique et constitue la voie de communication neuronale directe entre l’intestin et le cerveau 9. Ce nerf crânien le plus long du corps humain supervise une multitude de fonctions corporelles cruciales, incluant le contrôle de l’humeur, la réponse immunitaire, la digestion et la fréquence cardiaque.
Les AGCC activent directement le nerf vague, stimulant et facilitant la communication intestin-cerveau 7. Des études montrent que le butyrate augmente la vitesse à laquelle les neurones vagaux peuvent transmettre des signaux au cerveau, particulièrement les signaux de satiété. La stimulation des fibres afférentes vagales dans l’intestin influence les systèmes monoaminergiques du tronc cérébral qui jouent des rôles cruciaux dans les troubles psychiatriques majeurs, comme les troubles de l’humeur et anxieux 10.
Des recherches révolutionnaires ont démontré que certaines souches probiotiques, comme Lactobacillus rhamnosus, n’exercent pas d’effets anxiolytiques chez les modèles animaux lorsque le nerf vague est sectionné 11. De plus, la fonction vagale corrèle avec la diversité du microbiote intestinal, et les producteurs d’acides gras à chaîne courte, tels que Lactobacillales et Ruminococcaceae, sont plus abondants chez les individus présentant une meilleure fonction vagale 11.
Le nerf vague possède également des propriétés immunomodulatrices remarquables. Il régule une voie anti-inflammatoire cholinergique qui atténue l’inflammation et diminue la perméabilité intestinale 11, deux facteurs particulièrement pertinents dans le sous-type inflammatoire de la dépression.
Les preuves cliniques : probiotiques et santé mentale
L’accumulation de preuves cliniques concernant l’efficacité des probiotiques dans le traitement des troubles anxieux et dépressifs est impressionnante. Une méta-analyse récente publiée en 2024 a examiné 45 essais cliniques randomisés incluant 4 053 participants et dix types d’interventions 12. Les résultats révèlent que Bifidobacterium présente la plus grande probabilité d’être l’espèce probiotique optimale pour améliorer les symptômes anxieux (différence moyenne standardisée = -0,80 ; IC à 95% -1,49 à -0,11), suivi de Lactobacillus (DMS = -0,49 ; IC à 95% -0,85 à -0,12).
Une autre méta-analyse exhaustive portant sur les effets des probiotiques et prébiotiques sur la dépression et l’anxiété en 2024 a démontré des réductions significatives des symptômes dépressifs (DMS : -0,96 ; IC à 95% : -1,31, -0,61) et des réductions modérées des symptômes anxieux (DMS : -0,59 ; IC à 95% : -0,98, -0,19) 13.
Un essai clinique randomisé contrôlé publié dans Nature Translational Psychiatry en 2022 a testé le potentiel d’une supplémentation probiotique à haute dose de courte durée comme traitement adjuvant de la dépression 14. Les résultats ont montré une amélioration plus forte des symptômes dépressifs après la supplémentation probiotique, avec un taux de rémission de 55% dans le groupe probiotique comparé à 40% dans le groupe placebo lors du suivi à huit semaines. Cette étude a également détecté des changements dans le microbiome intestinal et des modifications neurales mesurées par imagerie cérébrale.
Les mécanismes d’action des probiotiques sont multiples. Les souches du genre Lactobacillus peuvent améliorer l’intégrité de la barrière intestinale, améliorer la tolérance immunitaire, réduire la translocation bactérienne et apporter des effets bénéfiques sur les comportements liés à l’anxiété et à la dépression 14. Ces bactéries produisent des AGCC tels que l’acétate, le butyrate et le propionate, qui jouent un rôle important dans le maintien de la santé de l’hôte et exercent des effets bénéfiques sans induire de remodelage du microbiome intestinal 14.
Inflammation, dysbiose et troubles mentaux
La dysbiose intestinale, définie comme un déséquilibre dans la composition du microbiome, perturbe l’axe intestin-cerveau et aggrave les symptômes dépressifs 15. Plusieurs facteurs peuvent causer ce déséquilibre, notamment le régime alimentaire, les antibiotiques et le mode de vie, entraînant des changements dans la composition microbienne, le métabolisme et les réponses immunitaires.
Les AGCC dérivés du microbiote intestinal jouent un rôle vital dans les actions anti-inflammatoires grâce à leur maintien de la perméabilité intestin-cerveau et à leur contribution constante au système nerveux central pour l’homéostasie de la microglie 6. Les AGCC, en particulier l’acétate, le propionate et le butyrate, ont été rapportés pour exercer des effets protecteurs sur la barrière intestinale en tant que substrats énergétiques. Le butyrate améliore l’expression des récepteurs des hydrocarbures aromatiques et du facteur 1α inductible par l’hypoxie, qui régulent à la hausse les niveaux d’IL-12, une cytokine protectrice qui contribue à résister aux stimuli inflammatoires et à maintenir l’homéostasie intestinale 6.
Des études ont démontré que les patients atteints de plusieurs troubles mentaux, dont la dépression et l’anxiété, présentent des altérations de leur microbiome intestinal 16. Une analyse récente a révélé que la sévérité des symptômes dépressifs corrèle positivement avec les niveaux d’acétate et négativement avec les niveaux de butyrate 17.
Implications nutritionnelles : nourrir le microbiome pour nourrir l’esprit
L’alimentation représente le facteur modifiable le plus puissant influençant la composition du microbiome intestinal. Le Dr Spencer recommande à ses patients de « prioriser une alimentation riche en aliments entiers et végétaux et d’éviter les produits transformés et ultra-transformés, qui sont riches en additifs et conservateurs pouvant perturber les bactéries saines de l’intestin » 1.
Les aliments riches en fibres constituent le substrat essentiel pour la production d’AGCC. Les régimes alimentaires riches en fibres incluent les légumes et fruits tels que oignons, haricots, brocoli, pommes, baies et avocats 8. Les oligosaccharides contenus dans ces fibres ne sont pas facilement digestibles mais servent de nourriture pour les microbes intestinaux, qui les fermentent pour produire des AGCC.
Les aliments fermentés – yogourt, kéfir, choucroute et kimchi – peuvent introduire directement des probiotiques bénéfiques dans l’intestin 18. Les acides gras oméga-3, présents dans les poissons gras comme les sardines, maquereaux et saumons, ont été démontrés pour augmenter la diversité des bactéries intestinales et spécifiquement augmenter les familles de bactéries produisant des AGCC 7.
Une analyse exhaustive des études reliant la nutrition aux troubles de santé mentale révèle que les interventions diététiques peuvent exercer des effets thérapeutiques sur les conditions neurologiques chroniques 19. Les prébiotiques, composants alimentaires utilisés par les micro-organismes intestinaux pour promouvoir la croissance et l’activité des bactéries bénéfiques, incluent les fructanes et les oligosaccharides dérivés du glucose. Bien que non absorbés par le corps humain, les prébiotiques sont fermentés par les bactéries intestinales bénéfiques, produisant des métabolites avantageux comme les AGCC 19.
Perspectives thérapeutiques innovantes : stimulation du nerf vague
Au-delà des interventions nutritionnelles et probiotiques, la stimulation du nerf vague (SNV) émerge comme une approche thérapeutique prometteuse pour les troubles psychiatriques résistants au traitement. La SNV applique des impulsions électriques au nerf vague, modulant ainsi les systèmes de communication intestin-cerveau 9.
Des preuves préliminaires suggèrent que la SNV constitue un traitement d’appoint prometteur pour la dépression résistante au traitement, le trouble de stress post-traumatique et les maladies inflammatoires de l’intestin 9. Les traitements ciblant le nerf vague augmentent le tonus vagal et inhibent la production de cytokines, deux mécanismes importants de résilience.
Une revue récente publiée en 2024 souligne que les déséquilibres dans le microbiome intestinal, tels que la dysbiose, peuvent altérer les voies de communication entre l’intestin et le cerveau, contribuant au développement de troubles neuropsychologiques 20. La SNV montre un potentiel pour moduler ces systèmes interconnectés, aidant à rétablir l’équilibre. De manière intéressante, la composition du microbiome intestinal peut également influencer l’efficacité de la SNV, car elle a le potentiel de modifier la réponse du cerveau à cette approche thérapeutique.
Des techniques non-invasives de SNV transcutanée se développent également, offrant une alternative aux dispositifs implantés chirurgicalement. Parallèlement, des pratiques corps-esprit comme la méditation et le yoga augmentent le tonus vagal et peuvent contribuer à la résilience et à l’atténuation des symptômes d’humeur et d’anxiété 10.
Développement précoce et fenêtres critiques
L’importance du microbiome dans la santé mentale commence dès la vie prénatale. On estime que plus de la moitié de l’énergie maternelle disponible pour le fœtus en croissance pendant la grossesse est allouée au développement cérébral 21. Le régime alimentaire joue un rôle critique dans le développement du microbiote intestinal dans la petite enfance. La recherche a démontré que la présence d’allaitement maternel ou de formule, ainsi que le moment de transition vers les aliments solides, sont des facteurs majeurs influençant le passage du microbiote intestinal vers une composition plus proche de celle d’un adulte 21.
Une explication de la relation entre le développement neurologique postnatal et la diversité du microbiote intestinal pourrait résider dans leur influence mutuelle sur leurs processus de maturation respectifs, médiée par l’axe microbiome-intestin-cerveau 21. Cette compréhension souligne l’importance d’interventions nutritionnelles précoces pour optimiser à la fois le développement du microbiome et la santé mentale à long terme.
Limites actuelles et directions futures
Malgré les avancées remarquables dans la compréhension de l’axe microbiome-intestin-cerveau, plusieurs limitations persistent. Bien que l’axe microbiome-intestin-cerveau soit de plus en plus reconnu comme une cible thérapeutique potentielle, davantage de recherches sont nécessaires pour combler les lacunes dans notre compréhension de son rôle dans la santé mentale 3. Une grande partie de la littérature existante s’appuie sur des modèles animaux, qui peuvent ne pas refléter fidèlement la physiologie humaine.
Les effets à long terme des interventions diététiques, des prébiotiques et des probiotiques sur la stabilité du microbiome intestinal et la santé globale sont encore en cours d’investigation 3. Pour mieux exploiter le potentiel thérapeutique des traitements basés sur le microbiome, les approches de médecine personnalisée devraient être prioritaires, intégrant le profilage du microbiome et d’autres biomarqueurs pour adapter les interventions aux patients individuels.
La recherche extensive actuelle dans le domaine probiotiques-santé mentale devrait se concentrer sur le mécanisme exact de fonctionnement des probiotiques, le dosage optimal, la durée optimale du traitement et les résultats potentiellement différents selon la sévérité de l’anxiété et de la dépression 22. De plus, il reste à déterminer si les probiotiques peuvent être utilisés comme traitement complémentaire combiné avec des antidépresseurs ou comme traitement primaire de la dépression.
Conclusion : vers une psychiatrie intégrative
La recherche sur l’axe microbiome-intestin-cerveau ouvre une nouvelle ère dans la compréhension et le traitement des troubles mentaux. Les découvertes scientifiques récentes démontrent de manière convaincante que notre santé mentale ne dépend pas uniquement de processus neurochimiques cérébraux isolés, mais résulte d’interactions complexes entre notre système nerveux central, notre système immunitaire, notre système endocrinien et les billions de micro-organismes qui habitent notre intestin.
Les probiotiques pourraient fournir une approche non médicamenteuse dans le traitement des troubles de l’humeur, aidant à élargir les options thérapeutiques pour les patients psychiatriques et non psychiatriques, tout en étant sûrs et bien tolérés 22. En tant que suppléments nutritionnels, les probiotiques pourraient également aider à atténuer la stigmatisation sociale rencontrée par les personnes prenant des médicaments psychotropes.
Cette approche intégrative, considérant la personne dans sa globalité plutôt que des systèmes organiques isolés, représente un retour à une vision plus holistique de la médecine. Comme l’a souligné une étude récente, l’idée d’étudier les processus de maladie nécessite de considérer la personne entière au lieu d’un ou deux systèmes organiques séparés 3.
Pour les cliniciens et les patients, ces découvertes offrent de nouvelles perspectives concrètes : optimiser l’alimentation en privilégiant les fibres et les aliments fermentés, considérer l’usage approprié de probiotiques spécifiques, pratiquer des techniques de gestion du stress qui soutiennent le tonus vagal, et reconnaître que la santé mentale commence dans l’intestin.
Alors que la recherche continue d’élucider les mécanismes complexes régissant ces interactions, l’avenir de la psychiatrie pourrait bien résider dans une approche qui intègre la nutrition, la modulation du microbiome, les thérapies conventionnelles et les interventions bioélectroniques comme la stimulation du nerf vague. Cette révolution scientifique transforme notre compréhension fondamentale de ce que signifie être humain, révélant que nous sommes non pas des individus isolés mais des écosystèmes vivants en interaction constante avec les micro-organismes qui nous habitent.
Références
- Stanford University Longevity Center. (2024). More Than a Gut Feeling: How Your Microbiome Affects Your Mood. https://longevity.stanford.edu/lifestyle/2024/04/08/more-than-a-gut-feeling-how-your-microbiome-affects-your-mood/
- Appleton, J. (2018). The Gut-Brain Axis: Influence of Microbiota on Mood and Mental Health. Integrative Medicine (Encinitas), 17(4), 28-32. https://pmc.ncbi.nlm.nih.gov/articles/PMC6469458/
- Jiang, M., et al. (2025). Microbiome Gut-Brain-Axis: Impact on Brain Development and Mental Health. Molecular Neurobiology. https://link.springer.com/article/10.1007/s12035-025-04846-0
- MDPI. (2024). Mind, Mood and Microbiota—Gut–Brain Axis in Psychiatric Disorders. International Journal of Molecular Sciences, 25(6), 3340. https://www.mdpi.com/1422-0067/25/6/3340
- Silva, Y.P., et al. (2020). The Role of Short-Chain Fatty Acids From Gut Microbiota in Gut-Brain Communication. Frontiers in Endocrinology, 11, 25. https://pmc.ncbi.nlm.nih.gov/articles/PMC7005631/
- Zhou, Z., et al. (2024). Gut microbiota-derived short-chain fatty acids and depression: deep insight into biological mechanisms and potential applications. Translational Psychiatry. https://pmc.ncbi.nlm.nih.gov/articles/PMC10882305/
- Psychology Today. (2024). Short-Chain Fatty Acids. https://www.psychologytoday.com/us/basics/short-chain-fatty-acids
- Park Compounding. (2022). Short Chain Fatty Acids and Mental Health – The Gut-Microbiota-Brain Axis. https://www.parkcompounding.com/short-chain-fatty-acids-and-mental-health/
- Breit, S., et al. (2018). Vagus Nerve as Modulator of the Brain–Gut Axis in Psychiatric and Inflammatory Disorders. Frontiers in Psychiatry, 9, 44. https://pmc.ncbi.nlm.nih.gov/articles/PMC5859128/
- Breit, S., et al. (2018). Vagus Nerve as Modulator of the Brain-Gut Axis in Psychiatric and Inflammatory Disorders. Frontiers in Psychiatry, 9, 44. https://www.frontiersin.org/journals/psychiatry/articles/10.3389/fpsyt.2018.00044/full
- Misiak, B., et al. (2023). Gut-brain-crosstalk- the vagus nerve and the microbiota-gut-brain axis in depression. A narrative review. Neuroscience Applied, 2, 101093. https://www.sciencedirect.com/science/article/pii/S2666915323001464
- Yang, Y., et al. (2024). Assessment of optimal combinations of therapeutic probiotics for depression, anxiety, and stress. Psychological Medicine, 54(10), 2547-2561. https://www.cambridge.org/core/journals/psychological-medicine/article/abs/assessment-of-optimal-combinations-of-therapeutic-probiotics-for-depression-anxiety-and-stress/F8A9A88CC8DC2E5689BB01E31B16E26E
- Nutrition Reviews. (2025). Effects of Prebiotics and Probiotics on Symptoms of Depression and Anxiety in Clinically Diagnosed Samples. https://academic.oup.com/nutritionreviews/advance-article/doi/10.1093/nutrit/nuae177/7934047
- Nikolova, V.L., et al. (2022). Clinical, gut microbial and neural effects of a probiotic add-on therapy in depressed patients: a randomized controlled trial. Translational Psychiatry, 12, 227. https://www.nature.com/articles/s41398-022-01977-z
- Patel, R.A., et al. (2024). Gut microbiome-gut brain axis-depression: interconnection. Current Psychology. https://pubmed.ncbi.nlm.nih.gov/39713871/
- Ghosh, T.S., et al. (2024). Gut-Brain Axis: Role of Microbiome, Metabolomics, Hormones, and Stress in Mental Health Disorders. Cells, 13(17), 1436. https://www.mdpi.com/2073-4409/13/17/1436
- Rizzetto, L., et al. (2024). Short-Chain Fatty Acids and Human Health: From Metabolic Pathways to Current Therapeutic Implications. Life, 14(5), 559. https://www.mdpi.com/2075-1