Le trouble déficitaire de l’attention avec hyperactivité (TDAH) est un trouble neurodéveloppemental caractérisé par hyperactivité motrice, déficit de l’attention et impulsivité, dont l’impact clinique est significatif. Sa prévalence atteint environ 5 % chez les enfants et 2,5 % chez les adultes. On admet que sa base étiologique est fortement génétique, avec une héritabilité estimée à environ 74 %. Les variantes génétiques communes contribuent chacune faiblement au risque, mais des variantes rares, de fréquence faible, peuvent avoir des effets plus marqués.
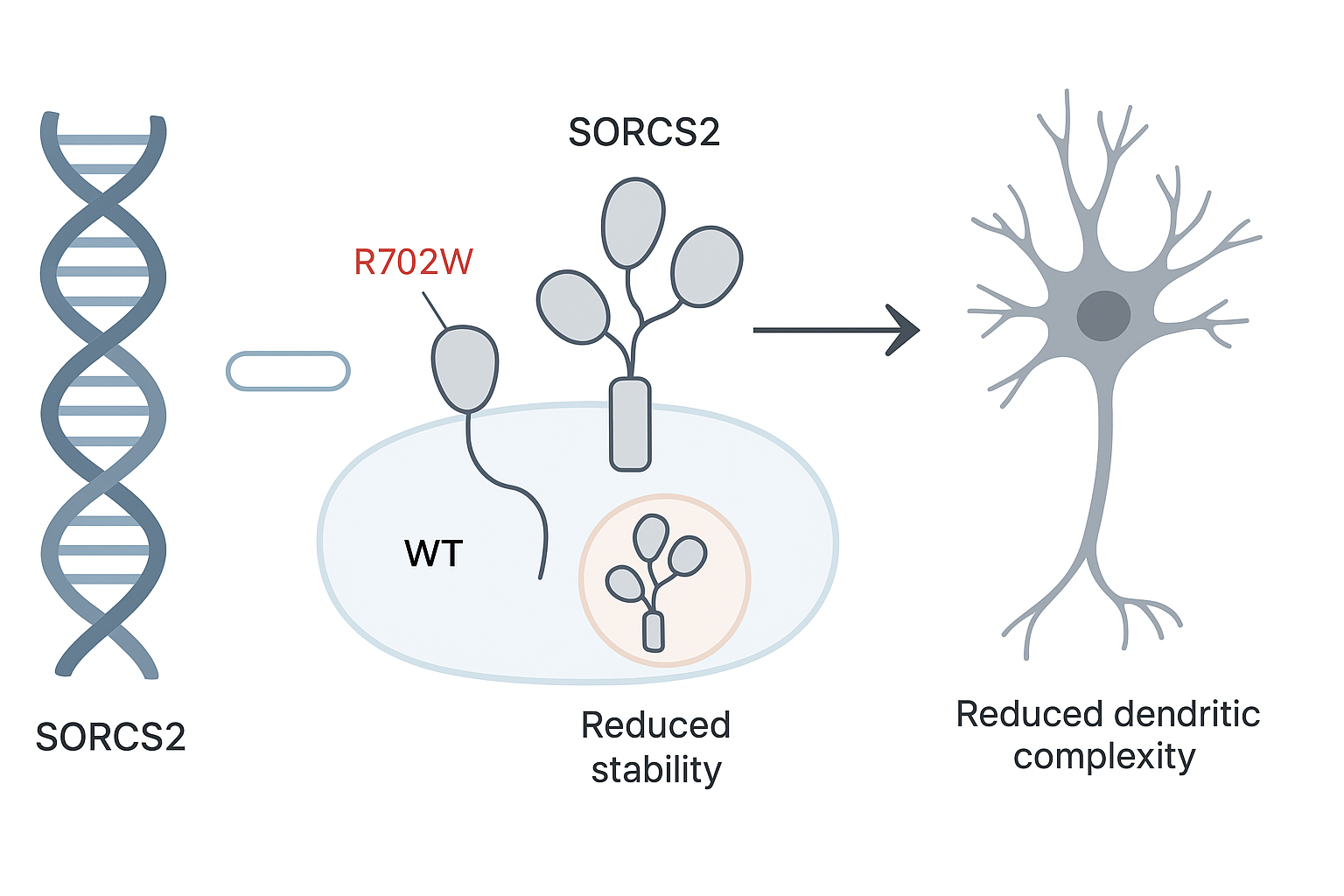
La protéine SorCS2, membre de la famille des récepteurs à domaine Vps10p (avec sortilin, SorLA, SorCS1 et SorCS3), joue un rôle crucial dans le développement neuronal, dans la plasticité synaptique, particulièrement via la modulation du signal du BDNF (Brain-Derived Neurotrophic Factor). Des travaux antérieurs sur des souris dépourvues de Sorcs2 montrent des comportements rappelant certains traits observés chez des patients atteints de TDAH, notamment hyperactivité, déficits cognitifs, réponses paradoxales aux stimulants.
L’étude présente l’identification d’une variante de SORCS2 à faible fréquence, dans une famille norvégienne présentant plusieurs cas de TDAH persistant, et caractérise les conséquences moléculaires, structurales et fonctionnelles de cette variante. L’objectif est d’éclairer comment une mutation rare dans SORCS2 peut contribuer au risque de TDAH, en altérant la stabilité du récepteur, sa localisation cellulaire et son activité dans la signalisation au BDNF.
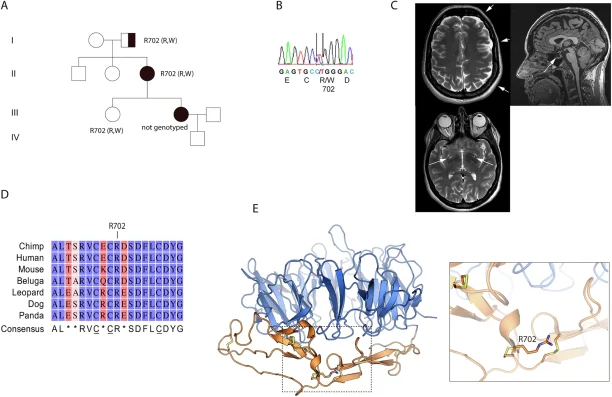
Identification de la variante R702W dans SORCS2
Les auteurs ont réalisé un séquençage de l’exome sur 21 familles norvégiennes avec plusieurs individus présentant un TDAH persistant. Dans l’une de ces familles, ils ont repéré chez trois individus un remplacement hétérozygote dans le gène SORCS2 : un changement nucléotidique dans l’exon 16 (4-7716081 C → T), se traduisant par une substitution d’un acide aminé : arginine (R) en position 702 → tryptophane (W), désigné R702W. Parmi ces trois porteurs, deux sont diagnostiqués TDAH, le troisième non. L’allèle est très rare (fréquence dans la base gnomAD ~ 0,000025).
Le résidu R702 est extrêmement conservé au cours de l’évolution, appartient au module 10CC de la zone extracellulaire du domaine Vps10p, un domaine structurel important doté de ponts disulfures, qui assure la stabilité de la conformation du domaine Vps10p. La localisation de R702 près de ces ponts disulfures suggère que sa substitution pourrait compromettre structure et repliement.
Effets moléculaires de la variante R702W sur le traitement post-tradutionnel, la maturation, la localisation et le transport cellulaire
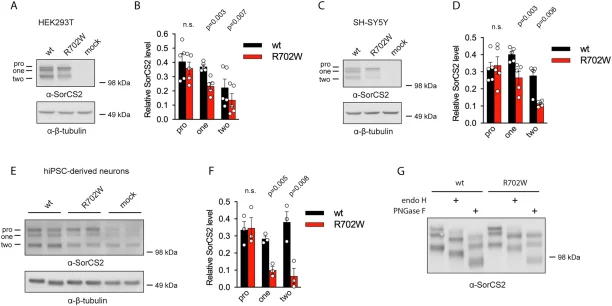
Les auteurs comparent la protéine SorCS2 version sauvage (WT) et la version mutant R702W dans divers systèmes cellulaires : lignées humaines (HEK293T, SH-SY5Y), neurones dérivés de iPSC (induit pluripotent stem cell), et neurones primaires de souris knockout pour Sorcs2.
Ils observent que la forme mature simple chaine et la forme en deux chaines de SorCS2 (formes traitées post-transcriptionnellement) sont significativement diminuées dans le mutant R702W, par rapport à la forme sauvage, dans tous les modèles cellulaires testés. En revanche, la forme pro-SorCS2 (non mature) est relativement préservée.
L’analyse de la glycosylation révèle que le mutant semble retenir des oligosaccharides de type high-mannose, ce qui suggère qu’il ne passe pas efficacement le contrôle qualité du réticulum endoplasmique (RE), ni le traitement normal de maturation (par ex. passage dans le Golgi).
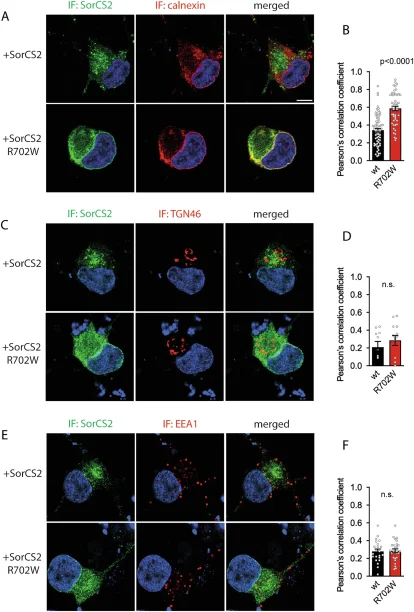
L’immunofluorescence montre que SorCS2 R702W s’accumule dans le RE (co-localisation accrue avec calnexine), et est moins présent à la surface cellulaire, alors que la version sauvage montre un transport normal jusqu’à la surface. Les marquages pour marqueurs du Golgi trans (TGN46) ou des endosomes précoces (EEA1) montrent moins de co-localisation pour le mutant, mais des analyses quantitatives suggèrent néanmoins une certaine présence dans ces compartiments.
Une fractionnement par centrifugation en gradient de densité confirme que la version R702W est en excès dans les fractions à forte densité correspondant au RE, tandis que les formes matures de SorCS2 WT prédominent dans les fractions de densité plus faible, incluant la surface cellulaire. Un test de biotinylation de protéines de surface confirme la réduction de SorCS2 R702W à la surface cellulaire.
Par ailleurs, une mesure du stress du RE (via l’augmentation de l’ARN du marqueur GRP78) suggère que la cellule prend en charge une charge protéique mal repliée, ce qui est cohérent avec l’accumulation du mutant dans le RE.
Instabilité protéique et clivage aberrant
L’étude montre que le domaine extracellulaire (ECD) purifié du mutant R702W est sujet à une dégradation plus prononcée pendant la purification, ce qui indique une instabilité du domaine. De plus, des fragments de la protéine mutant sont présents dans des fractions à forte densité, ce qui suggère que la protéolyse commence tôt, possiblement dans le RE ou dans des compartiments intracellulaires, avant même que la protéine n’atteigne le compartiment de surface.
Un marquage métabolique pulse-chase indique que le mutant R702W libère davantage de domaine extracellulaire (ECD) dans le milieu extracellulaire comparativement au WT, ce qui est interprété comme un « shedding » accru, une coupure protéolytique libérant le domaine extracellulaire. Ce shedding du WT est inhibé par un inhibiteur métallique (galardin), mais pas celui du mutant, indiquant que le mutant est clivé par des protéases différentes ou selon une modalité différente.
Une mesure du niveau de SorCS2 ECD sérique (via ELISA) chez un individu porteur dont le TDAH est diagnostiqué montre une valeur de ~ 26,1 ng/ml, comparée à une médiane de ~ 16,3 ng/ml chez les témoins, suggérant que cette libération extracellulaire anormale pourrait se manifester dans des fluides biologiques.
Effet dominant négatif sur la signalisation BDNF
La protéine SorCS2 fonctionne en formant des homo-dimères et des hétéro-dimères (notamment avec SorCS3). Les expériences montrent que le mutant R702W conserve la capacité de former des dimères avec lui-même et avec la version sauvage de SorCS2, ainsi qu’avec SorCS3. Ce qui signifie que le mutant pourrait interférer avec la fonction de la forme sauvage via hétéro-complexes.
Dans des neurones de souris knockout pour Sorcs2, la transfection avec la version WT seul permet sensible-ment de restaurer une réponse à la stimulation par BDNF (augmentation de la complexité des branches dendritiques), tandis que le mutant R702W n’induit pas cette réponse. De plus, dans une configuration hétérozyote (co-transfection WT + R702W), le mutant semble abroger la fonction de la forme sauvage, ce qui montre un effet dominant négatif.
Autres variantes rares dans SORCS2 et leur impact fonctionnel
En plus de R702W, les auteurs examinent d’autres variantes à faible fréquence identifiées dans deux cohortes (norvégienne, allemande/pays‐Bas) (nombre de cas TDAH vs témoins). Au total, 38 variants missense dans les cas TDAH et 65 chez les témoins selon les critères de fréquence. L’analyse bioinformatique (SIFT, PolyPhen-2, CADD-PHRED, MutationTaster, AlphaMissense, MPC) ne recense pas une surreprésentation statistiquement significative des variants jugés « dommageables » chez les patients vs témoins (p = 0,55).
Cependant, certains variants sélectionnés (S484I, R631C, R666C) montrent, lorsqu’ils sont fonctionnellement testés, des altérations de la liaison au ligand (proBDNF), de la capacité de formation de dimères, ou de localisation subcellulaire. Tous ces variants, comme R702W, sont incapables de restaurer la réponse BDNF dans les neurones knockout, ce qui suggère que de multiples substitutions dans le domaine Vps10p de SorCS2 perturbent sa fonction, même si leur contribution au risque de TDAH au niveau populationnel reste incertaine.
Cohérence clinique et imagerie
Dans la famille porteuse de R702W, l’imagerie cérébrale (IRM T1 pondéré) de l’un des porteurs diagnostiqués ne montre pas de lésions structurelles nettes : structures internes, ganglions de la base, cervelet sont jugés normaux, seules quelques asymétries du cortex, des espaces perivasculaires élargis et une sella partiellement vide sont observées. Ceci suggère que la variante ne provoque pas de malformations majeures, mais pourrait entraîner des modifications plus subtiles ou fonctionnelles.
Le fait qu’un porteur ne soit pas diagnostiqué TDAH souligne que la pénétrance du variant pourrait être incomplète, dépendant du contexte génétique (charge polygénique) et environnemental. Ce point est mis en avant par les auteurs comme limite importante.
Interprétation structurale
Le domaine 10CC, module du domaine Vps10p, contient cinq ponts disulfures très conservés. Le résidu R702 est proche spatialement de deux de ces ponts, ce qui laisse penser que sa substitution par W pourrait perturber la formation ou la stabilité de ces liaisons, affectant le repliement du domaine, le passage du RE au Golgi, et l’intégrité structurelle de l’interaction avec les ligands (BDNF/proBDNF) ou avec d’autres protéines SorCS.
Cette altération structurelle se traduit par un défaut de traitement post-tradutionnel, une rétention dans le RE, une instabilité du domaine extracellulaire, un clivage non spécifique, et une perte (ou réduction) de la fonction de signalisation.
Implications pour la physiopathologie du TDAH et perspectives
Cette étude démontre qu’une variante rare dans SORCS2 peut compromettre de façon significative la stabilité, le trafic, la maturation et la fonction d’un récepteur impliqué dans la signalisation neurotrophique. Elle suggère qu’au sein du large spectre génétique du TDAH, les variants rares à effet modéré ou fort peuvent contribuer à des cas familiaux avec TDAH persistant.
L’effet dominant négatif du variant R702W signifie qu’il ne suffit pas que l’allèle muté soit présent : il peut aussi nuire à l’allèle normal, aggravant l’atteinte.
Sur le plan thérapeutique, bien que cette recherche soit encore fondamentale, elle appelle à examiner si des interventions visant à restaurer la maturation du récepteur, à réduire le stress du RE ou à moduler la signalisation du BDNF pourraient avoir un intérêt dans des sous-groupes de patients porteurs de tels variants.
Enfin, l’étude appelle à étendre le séquençage des cohortes, à améliorer la précision des études fonctionnelles pour d’autres variants, et à établir des corrélations plus détaillées genotype–phénotype.
Critique et limites
Premièrement, la taille de la famille étudiée pour R702W est modeste, et un porteur ne présente pas le phénotype TDAH, ce qui complique la preuve de causalité stricte. L’absence de ségrégation claire limite le degré de certitude.
Deuxièmement, bien que l’étude fonctionnelle soit très poussée, les modèles cellulaires in vitro ou ex vivo, ou les neurones de souris knockout, restent des approximations du contexte humain. Les effets du variant pourraient être modulés dans le cerveau humain en fonction de l’environnement, des autres gènes, du moment de l’expression.
Troisièmement, l’absence d’une surreprésentation statistique nette des variants « dommageables » dans SORCS2 parmi les patients vs témoins suggère que ces variants rares ne sont pas un facteur majeur de risque pour toute la population TDAH, mais plutôt peut-être pour des cas individuels ou familiaux.
Quatrièmement, l’IRM montre peu de changements structurels, ce qui suggère que les conséquences de la variante peuvent être fonctionnelles plus que structurelles, et donc difficiles à détecter via imagerie conventionnelle.
Conclusion
L’étude identifie une variante rare (R702W) dans le gène SORCS2 chez une famille avec plusieurs membres atteints de TDAH persistant. Elle démontre que cette mutation entraîne des perturbations multiples : repliement du domaine, traitement post-traditionnel, localisation cellulaire, instabilité extracellulaire, clivage anormal, et perte de capacité à transmettre la signalisation induite par le BDNF. En outre, le mutant exerce un effet dominant négatif sur l’allèle sauvage, ce qui peut amplifier ses effets pathologiques. Bien que les preuves de contribution de SORCS2 à la charge globale génétique du TDAH restent limitées, ce travail enrichit notre compréhension des mécanismes moléculaires potentiellement impliqués dans certains cas de TDAH et ouvre la voie à des explorations thérapeutiques ciblées.